Наконец-то создатели «Спутника V» опубликовали исследование этой вакцины. Главный вывод — она безопасна и очень эффективна (но вопросы остались)
Институт Гамалеи опубликовал промежуточные результаты исследования третьей фазы по эффективности, безопасности и иммуногенности вакцины «Cпутник V». Ранее были доступны результаты только из пресс-релизов спонсора разработчика, Российского фонда прямых инвестиций (РФПИ) и «народного исследования» в телеграме.
Что стало известно
- В рамках исследования с 7 сентября по 24 ноября 14 964 участника получили две дозы вакцины и 4902 — плацебо. Период наблюдения на момент анализа промежуточных результатов составил 48 дней после первой инъекции (интерквартильный интервал 39–58). Окончательный анализ еще впереди, он предусматривает анализ числа случаев заболевания в течение 180 дней после второй инъекции.
- В первоначальном протоколе не планировалось промежуточных анализов, однако в связи с ростом случаев 5 ноября в протокол были внесены изменения о промежуточных анализах при накоплении 20, 39 и 78 случаев заболевания.
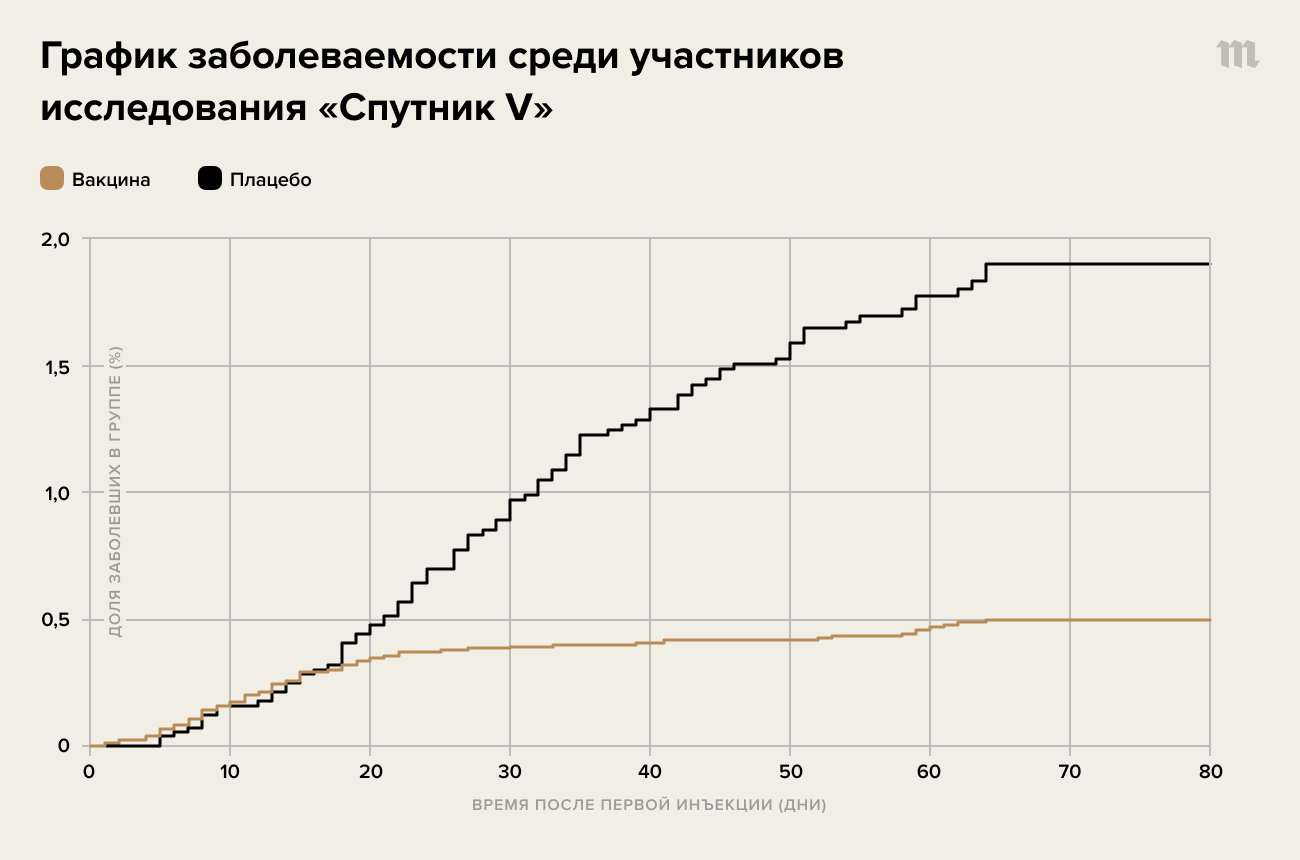
- В группе вакцины заболело 16 человек (0,1%), в группе плацебо — 62 человека (1,3%). Таким образом, эффективность составила 91,6% (95%, доверительный интервал 85,6–95,2).
- Важно, что 1611 участников, получивших вакцину, были старше 60 лет (из них почти половина — с сопутствующими заболеваниями), и в этой категории эффективность не отличалась.
- Большая часть заболевания в группе вакцины происходит до второй инъекции, то есть защита становится заметной примерно на 16–18-й день.
- Все средние и тяжелые случаи после 21-го дня были в группе плацебо.
- У подавляющего большинства изученных участников (342 в группе вакцины, 114 в контроле) вакцина вызывала образование и связывающих, и нейтрализующих антител.
- Клеточный ответ регистрировался у всех (44 человек) изученных привитых, в отличие от непривитых (14 человек).
- 94% нежелательных явлений были легкими. Разбивка по ним между группами вакцины и плацебо в статье приводится, но, к сожалению, только для лиц старше 60 лет — в данных Pfizer и Moderna были приведены все группы. В группе вакцины ожидаемо больше случаев гриппоподобного синдрома, местных реакций, контактного дерматита, повышенной температуры.
- Частота серьезных нежелательных явлений не отличалась между группами, и ни одно серьезное нежелательное явление не было связано с вакцинацией, по мнению независимого комитета по мониторингу данных.
- В группе вакцины было две смерти от COVID-19. Пациенты заболели на 4-й и 5-й день после первой инъекции. Исследователи делают вывод, что умершие были заражены до начала исследования, хотя ПЦР и был отрицательным.
В целом можно сказать, что, по данным публикации, вакцина в краткосрочной перспективе высокоэффективна и безопасна. Как полученный иммунитет будет вести себя на длинном горизонте, пока сказать не может никто и ни для одной вакцины.
Как это соотносится с другими исследованиями
Единственное опубликованное исследование фазы III другой аденовирусной вакцины — это исследование вакцины AstraZeneca на основе аденовируса шимпанзе. Точнее, это публикация о четырех исследованиях в Великобритании, Бразилии и ЮАР, из которых исследование в Великобритании относится к совмещенной фазе II/III, а исследование в Бразилии — фазе III.
Вакцина вводится двумя дозами c интервалом 4–12 недель, эффективность оценивалась начиная с 14-го дня после второй дозы.
Общая эффективность у AstraZeneca составила 70,4%. В бразильском исследовании эффективность составила всего 64,2%. А вот в британском исследовании была подгруппа пациентов, получавшая первую дозу вдвое меньше второй. В этой подгруппе эффективность была 90%, а эффективность против бессимптомных случаев — 58,9%.
Так же, как и у «Спутника V», начиная с 21-го дня после первой дозы эффективность против тяжелых случаев составила 100%, то есть тяжело заболевших не было.
По вакцине компании Johnson & Johnson, которая представляет собой аналог первого компонента «Спутника V», недавно в виде пресс-релиза были опубликованы предварительные результаты. Эта вакцина вводится одним уколом, и уровень защиты через 28 дней после вакцинации оказался 72% в США, 66% в Латинской Америке и 57% в ЮАР. Вакцина показала 85% защиты от тяжелого заболевания, а спустя 49 дней после прививки защита составила 100%.
Значит, «Спутник V» эффективнее иностранных вакцин?
Прежде всего, важно понимать, что, помимо аденовирусных, есть другие типы вакцин (например, та же Pfizer/BioNTech). Но сравнение важно не для оценки конкурентных преимуществ каждой (на самом деле они очень похожи по эффективности), а чтобы понять, подходят ли аденовирусные вакцины для борьбы с ковидом в принципе.
Кроме того, надо заметить, что сравнивать результаты между исследованиями не совсем корректно, потому что у всех описанных исследований разный дизайн и разная выборка пациентов. Тот факт, что исследование «Спутника V» проводилось только в Москве, делает его выборку более однородной, чем в экспериментах AstraZeneca и J&J (начаты отдельные испытания в ОАЭ, Венесуэле и Индии, но их результатов придется еще подождать).
С чем связана более низкая эффективность вакцин AstraZeneca и J&J по сравнению со «Спутником V» — не вполне ясно. Причин может быть несколько:
- «Спутник V» благодаря использованию в качестве векторов двух разных аденовирусов (Ad26 и Ad5) действительно эффективнее конкурентов
- «Спутник V» исследовался на достаточно однородной выборке пациентов, не включал различные варианты коронавируса, от которых вакцина защищает хуже
- Исследование «Спутника» переоценивает его реальную эффективность из-за методологических недостатков и/или фальсификаций
У AstraZeneca и J&J промежуточные анализы были запланированы заранее, что более корректно с точки зрения научной целостности исследования, чем когда их добавляют в ходе исследования. Есть и некоторые несоответствия: в статье, например, говорится, что впервые базу данных об участниках исследования открыли для анализа 18 ноября, когда накопилось 20 случаев заболевания, но пресс-релиз об этом вышел еще 11 ноября. В результате возникает вопрос, чем это несоответствие объясняется и насколько тщательным было ослепление в ходе исследования — это может повлиять на результаты исследования.
Кроме того, необходимо отметить, что протокол исследования Института Гамалеи, в отличие от протоколов AstraZeneca и J&J, так и не опубликован, что затрудняет анализ результатов. В частности, не совсем понятно, как определялось, при каком сочетании симптомов нужно было отправлять участника исследования на ПЦР. Отсутствие четких критериев оставляет здесь пространство для (осознанного или нет) искажения результатов со стороны участвовавших в исследовании врачей. В случае «Спутника V» (впрочем, как и большинства остальных мировых вакцин) легко понять по симптомам, что получил человек: вакцину или плацебо. В таких условиях врачу становится легче манипулировать данными, если нет четкого алгоритма. Исключением можно считать исследование AstraZeneca — в нем в качестве контроля использовалась вакцина от менингококка, а не плацебо, поэтому «расслепить» такое исследование на уровне врачей труднее. К тому же для них был предусмотрен и четкий алгоритм определения, кого считать заболевшим.
Анализ также затрудняет отсутствие более подробных данных по сопутствующим заболеваниям в статье о «Спутнике V». Приведено только общее число таких людей в группе старше 60 лет, тогда как в статье AstraZeneca есть разбивка отдельно по сердечно-сосудистым заболеваниям, респираторным заболеваниям и диабету.
Что еще неизвестно
В дальнейшем при исследовании «Спутника V» необходимо получить более долговременные данные об эффективности и безопасности. В частности, нужно понять, сколько продержится защита от коронавирусной инфекции, которую обеспечивает вакцина. Вакцины, построенные на основе аденовирусных векторов, скорее всего, не получится вводить несколько раз: иммунный ответ на вектор воспрепятствует выработке ответа на белок коронавируса, по крайней мере в течение значительного времени после первой прививки. Требуется больше исследований на различных подгруппах: разные сопутствующие заболевания, беременные, кормящие, дети.
Также исследование пока не отвечает на вопрос, насколько вакцина эффективна в плане предотвращения бессимптомного носительства. Это нужно, чтобы понять, способна ли она замедлять пандемию или только снижает количество симптоматических и тяжелых больных (что тоже важно).
И наконец, очень интересно, насколько «Спутник V» защищает от новых вариантов коронавируса, таких как британский и южноафриканский. Для первого получены данные о большей заразности и большей тяжести заболевания, для второго — о потенциально меньшей эффективности вакцин Novavax, J&J и, возможно, Moderna.
Так или иначе, с учетом данных «народного исследования» специалисты сходятся на том, что риски заболеть коронавирусом намного выше рисков вакцинации, поэтому прививаться стоит как можно скорее тем, что есть. При этом по-прежнему следует соблюдать карантинные ограничения, потому что ни одна вакцина не защищает на сто процентов — они лишь существенно снижают риски заболеть симптоматически.
Илья Ясный