Сколько действует вакцина от COVID-19? Можно ли после прививки жить как раньше? Защитит ли она от новых штаммов?
Рассказываем, что известно о вакцинном иммунитете прямо сейчас
В мире уже есть как минимум пять вакцин против SARS-CoV-2, эффективность которых довольно надежно показана в масштабных исследованиях. Но остается важнейший вопрос: как долго будет длиться вакцинный иммунитет, не придется ли каждый год делать прививку заново? Опыт других заболеваний говорит о том, что в общем случае предсказать длительность иммунитета (например, по уровню антител) невозможно — для разных заболеваний ситуация развивается по-разному и важны разные компоненты иммунной системы. Несмотря на это, уже сейчас становится ясно, что в случае ковида с самим иммунитетом, скорее всего, все будет в порядке: главная проблема — это не «падающие антитела», а новые штаммы вируса, которые уже научились обманывать систему защиты организма.
Когда вакцина начинает действовать?
Все вакцины против коронавируса, по которым есть данные на сегодня, начинают действовать примерно спустя две-три недели после первого укола. Это хорошо видно просто по графикам заболеваемости среди вакцинированных и невакцинированных групп в клинических исследованиях: примерно две недели заболевшие накапливаются в обеих группах с одинаковой скоростью, а затем в вакцинированной группе наступает перегиб и люди начинают заболевать гораздо реже. Этот срок (две-три недели) соответствует среднему времени, за которое при вакцинации успевают в значительном количестве выработаться антитела, что косвенно подтверждает важность антител в защите от заболевания.
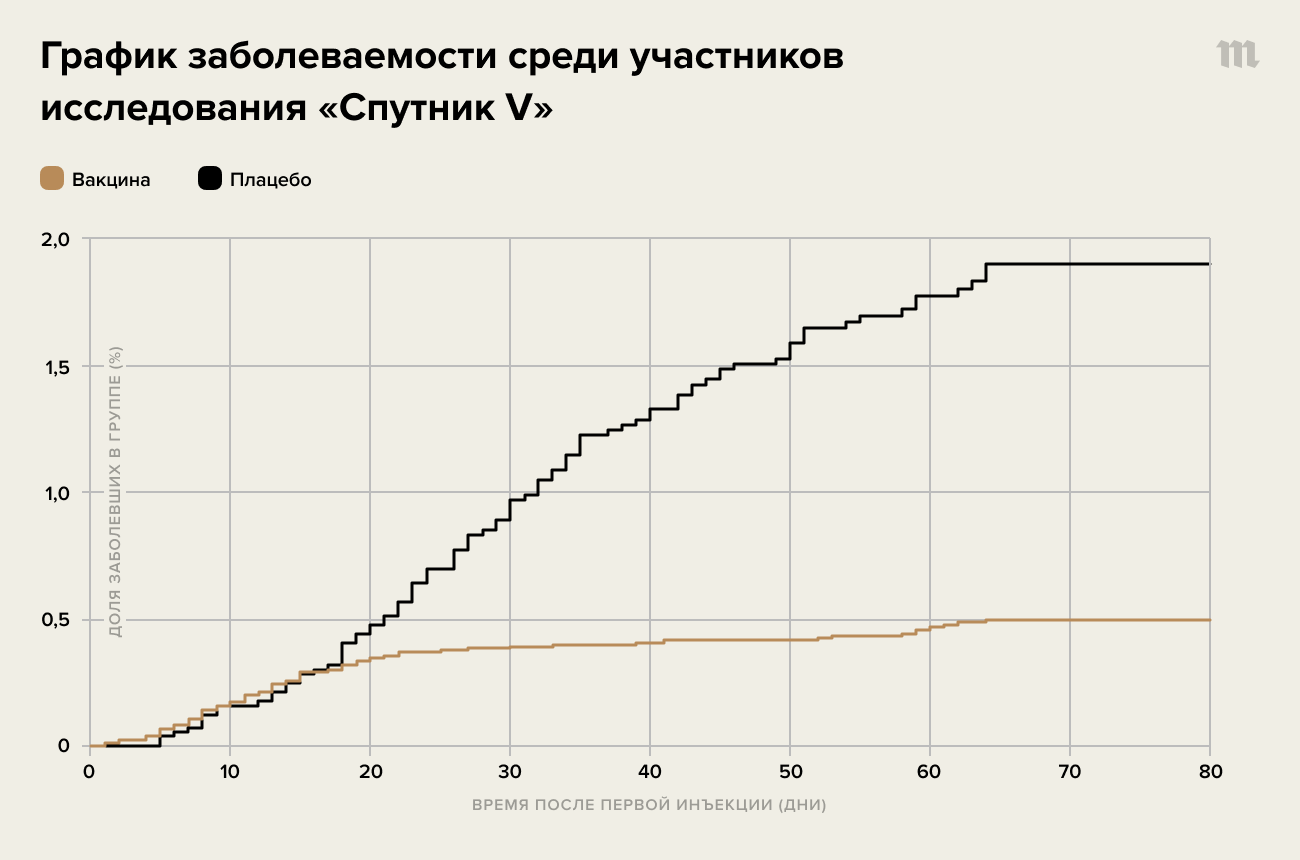
Такого рода графики есть для вакцин производства Moderna, Pfizer/BioNTech, J&J и «Спутника V». Они выглядят очень похоже друг на друга, за исключением, может быть, небольшой разницы в том, на какой именно день приходится этот перегиб. Различия между вакцинами, возможно, имеют какое-то интересное иммунологическое объяснение (например, связанное с разницей между вакцинными носителями — мРНК или аденовирусом), но в практическом плане они несущественны: нельзя сказать, что у всех вакцинированных именно на 18-й день происходят какие-то качественные изменения иммунитета, некое «включение тумблера защиты». Просто в среднем именно в этот момент снижается вероятность заболеть.
Хотя на картинках этого не видно, важно иметь в виду, что все они построены на данных людей, которые получили оба укола — и первый, и второй. Никаких следов усиленной защиты после второго укола (второго перегиба) мы на них не видим, но это не значит, что второй укол не нужен. Во-первых, не понятно, как выглядел бы график без него — хотя теоретически для «Спутника V» он должен воспроизводить соответствующий график (.pdf, стр. 60) для вакцины J&J, ведь она очень похожа на первый компонент «Спутника V». Во-вторых, созревание антител и изменение иммунного ответа после второй (бустерной) вакцинации может иметь отложенные последствия не сейчас, а через год или два — ведь известно, что при некоторых других заболеваниях без бустерной вакцинации иммунная память может быть нестабильной.
Можно ли заразиться между первым и вторым уколом? А заболеть после второго?
И то и другое возможно. Ни одна из сегодняшних вакцин не имеет 100%-ной эффективности, а это значит, что заболеть можно и после вакцинации, только с меньшей вероятностью. Для вакцины с эффективностью 90% эта вероятность в десять раз меньше вероятности заболеть без прививки, для вакцины с эффективностью 95% — в 20 раз меньше и так далее.
Что касается периода между уколами, то для подавляющего большинства вакцин он настолько короткий (21 или 28 дней), что проще исходить из того, что никакого иммунитета до второго укола вообще нет. Это будет некоторым упрощением действительности (вторая вакцинация почти, но не вполне совпадает с началом перегиба в графиках выше), но в практическом смысле вполне разумным.
Правда ли, что даже после вакцинации нужно соблюдать меры безопасности? Маски страшно надоели!
Соблюдать ограничения, когда в них нет практического смысла, действительно неприятно. Однако обратите внимание: то, что мы знаем об эффективности вакцин сегодня, относится только к снижению вероятности заболевания, а не вероятности инфекции — а это разные вещи.
Даже после вакцинации все еще можно стать бессимптомным носителем инфекции, не заметить этого и заразить кого-то другого. Про некоторые вакцины (например, полиомиелит, корь, краснуха) действительно известно, что они создают не только защитный, но и стерилизующий иммунитет, — в таком случае при попадании в организм человека вирус не размножается и не может передаваться от этого человека другим.
Но такой сценарий скорее исключение, а не правило в вакцинном мире. Попадают ли противоковидные вакцины в список таких счастливых исключений, которые создают стерилизующий иммунитет, сейчас мы не знаем. Исследования этого вопроса активно ведутся. Видимо, довольно скоро ученые точно измерят, насколько именно снижается вероятность заражения для вакцинированного человека по сравнению с тем, кто не сделал прививку, и вполне возможно, это снижение будет очень сильным — но до этого момента нужно еще дожить.
Пока же при принятии решений следует ориентироваться не на сам факт вакцинации, а на число потенциально опасных контактов и возможные последствия: даже если вы давно вакцинировались, не стоит навещать бабушку, если недавно вы побывали на концерте.
Прививка сделана, у меня высокий уровень антител. Значит, все в порядке?
Мы уже писали, что делать тест на антитела после вакцинации не нужно. Можем только повторить: если вы сделали прививку, то вакцина, скорее всего, подействовала и никакой тест к этому факту ничего не прибавит. Оговорка «скорее всего» здесь отражает личные особенности иммунной системы, о которых вы наверняка знаете сами (иммунодефицит, иммуносупрессивная терапия и т. д.).
Учитывая тот факт, что некоторые из вакцинированных все-таки заболевают, конечно, было бы здорово иметь какой-то тест, который сразу скажет, можете ли вы попасть в число заболевших или же полностью защищены. Но для этого ученым нужно сначала точно установить, что именно отличает заболевших вакцинированных от незаболевших: низкий ли это уровень антител или, может быть, их плохое «качество». А то и вовсе некая особенная история перенесенных ранее инфекций.
Так или иначе, пока таких «коррелятов защиты», то есть особенностей, которые указывают на вероятность заболевания, ученые для коронавирусных вакцин не нашли. Поиск этих коррелятов активно ведется — но пока приходится признать, что даже для старых, хорошо известных заболеваний знания о таких коррелятах весьма поверхностны и далеки от полноты.
Если антитела не гарантируют защиты, то что гарантирует?
Уровень антител, конечно, связан с уровнем защиты. Но только связь эта, как и все в иммунологии, не такая простая, как кажется. Существует целая отдельная область этой науки — исследование коррелятов защиты, — в рамках которой ученые пытаются установить, что именно в иммунной системе позволяет предсказать, что человек не заболеет, столкнувшись с тем или иным возбудителем. И в каких случаях заболевание все-таки развивается, даже если у человека был опыт столкновения с возбудителем. Стэнли Плоткин, автор одного из классических учебников по вакцинологии, называет эту область «одной из самых противоречивых в инфекционной медицине», при этом именно его обзоры коррелятов защиты являются самыми цитируемыми, и их можно рекомендовать для введения в тему коррелятов.
Да, один из основных коррелятов защиты — это антитела, они играют важную роль в случае большинства известных инфекций. Иногда самого по себе высокого уровня антител (например, полученного в ходе переливания сыворотки крови) вполне достаточно и ничего дополнительного не требуется. В таком случае обычно даже известен порог количества антител, после которого заболевания не случается.
Так, для гепатита A известно, что при уровне антител в плазме крови 10 международных единиц на миллилитр (10 mIU/mL) заболевание почти исключено. И это довольно низкий уровень — после вакцинации против этого заболевания уровень антител обычно в сотни раз превышает этот пороговый уровень. Защитный уровень антител был установлен, например, и при испытании (не очень удачно) вакцины от болезни Лайма: тогда ученые определили, что у всех, кто был вакцинирован, но все-таки заболел, уровень антител был существенно ниже среднего в 1100 единиц, то есть в их случае прививка не сработала. Больше ничем существенным заболевшие от незаболевших не отличались, поэтому и был сделан вывод о том, что дело исключительно в антителах.
Но чем подробнее ученые исследуют корреляты защиты, тем сложнее становится картина. Часто одного лишь суммарного уровня антител оказывается недостаточно для предсказания наличия или отсутствия защищенности. Например, для гриппа давно считается, что при общем титре антител 1:40 и выше заболевание обычно не происходит. Однако антитела против вируса могут быть разных типов, они могут присутствовать в крови или в слизистых, и не всегда можно угадать, какие из них «важнее».
Как раз в случае гриппа было показано, что это различие между типами антител оказывает существенное влияние на заболеваемость. Так, в исследовании на детях, которым давали живую противогриппозную вакцину, у тех, кто до вакцинации не имел совершенно никаких специфичных антител, ослабленный вакцинный вирус размножался в верхних дыхательных путях в 63% случаев (дети не заболевали, речь шла просто о размножении вируса). Среди тех, у кого в момент вакцинации в крови имелись только иммуноглобулины IgG, вирус размножался у 15%, а тех, кто был положителен на антитела IgA в секретах слизистой, эта доля составляла 19%. Однако если у ребенка присутствовали оба типа антител, даже не в очень большом количестве, они давали синергетический эффект: только у 3% таких детей иммунитет не был стерилизующим, то есть допускал размножение вируса. Если в случае нового заболевания будет наблюдаться подобная картина, то общий анализ на антитела будет не очень информативен — ведь для определения коррелята защиты важна будет именно разбивка по классам антител, дополненная способом интерпретации этих данных.
И это лишь отдельный пример важных различий, которые не фиксируют тесты, внутри единственного потенциального коррелята иммунной защиты — общего уровня антител. А ведь помимо них важнейшую роль для прогнозирования судьбы инфекции играют и состояние B-клеток памяти, которые хранят информацию об антителах и производят их при повторной инфекции, и T-клетки разных классов, помогающих или непосредственно участвующих в уничтожении зараженных вирусом клеток организма. Ну и другие компоненты иммунитета, в том числе и врожденного. Кроме того, часто критически важную роль в судьбе инфекции играет само количество вируса, которое попадает в организм, — это, например, установлено в случае полиомиелита.
В общем, все это говорит о том, что в иммунологии, к сожалению, нет единого и универсального параметра, измерения которого было бы достаточно для того, чтобы предсказать, есть ли у человека в данный момент достаточный для предотвращения заболевания иммунитет или нет. Хотя по отдельным болезням (например, тому же гепатиту А) многолетние наблюдения позволяют делать какие-то надежные прогнозы о том, заболеет ли человек, но в общем виде для нового заболевания вроде COVID-19 эта задача не имеет решения. На сегодня самые надежные данные по новой инфекции — это данные по испытаниям эффективности вакцин. Они, конечно, не дают никакой информации по каждому человеку отдельно, но позволяют утверждать что в среднем у вакцинированных вероятность заболеть в разы ниже, чем у невакцинированных.
Но хотя бы от тяжелого течения болезни вакцины точно защищают?
Да. Тут довольно просто — во всех опубликованных исследованиях среди вакцинированных (а это около 175 тысяч человек) не было случаев госпитализаций и смертей, связанных с ковидом (цифры можно посмотреть, например, тут). Умершие в таких больших группах, конечно, фиксировались, но эти смерти не были связаны с коронавирусной инфекцией. Уровень иммунного ответа у разных людей был очень разный, но поскольку в любом случае его было достаточно для профилактики тяжелого ковида, можно ожидать, что такая защита продлится долго.
Так почему вообще иногда иммунитет бывает пожизненным, а иногда нет?
То, насколько долго может продлиться иммунитет к возбудителю после болезни или вакцинации, зависит от двух очень разных вещей: стабильности иммунной памяти и скорости эволюционного изменения самого возбудителя. Это легко проиллюстрировать на примере того же гриппа.
Еще в 2008 году группа американских инфекционистов показала, что иммунная память может длиться очень долго и быть фактически пожизненной даже в случае такого вроде бы «эфемерного» заболевания, как грипп. Некоторое время до этого другие исследователи реконструировали последовательность генома испанского гриппа (он вызвал легендарную пандемию 1918 года), что позволило создать тест-системы, которые детектируют наличие антител именно к этому типу гриппа. Авторы статьи тогда нашли 32 человека, рожденных до 1915 года, провели анализ их крови и показали, что буквально каждый из них на момент исследования имел в крови антитела к испанке, хотя сам вирус уже 90 лет как исчез из человеческой популяции. Химически эти антитела, конечно, не были теми самыми белками, которые выработались когда-то в начале XX века: время полужизни самих антител как белковых молекул невелико и составляет примерно 21 день. Те антитела, которые удалось обнаружить в 2008 году, были синтезированы в организме переболевших долгожителей незадолго до самого эксперимента клетками памяти. Те сохранили специфичность к испанке и работали, судя по всему, в течение всей жизни, хотя и не сталкивались с вирусом и не могли быть им реактивированы почти столетие. Тем не менее появление новых вариантов гриппа требует ежегодной вакцинации, но это никак не связано с тем, что иммунитет к гриппу вдруг самостоятельно исчезает.
И это не исключение — подобная работа была сделана и для оспы, так что, в общем, возможность пожизненного иммунитета не вызывает у ученых беспокойства. Есть, конечно, случаи, когда даже у переболевших повторная инфекция становится возможна тем же возбудителем, что и в первый раз, но это всегда исключение, а не правило. Например, в норме вакцинацию против менингококка повторять не требуется, но в некоторых группах людей со сниженным иммунитетом ту же самую вакцину требуется вводить заново каждые пять лет или даже чаще.
Как бы то ни было, правило заключается в том, что иммунная память к конкретному возбудителю обычно остается долгой и часто бывает пожизненной, а вот возбудитель может меняться и уходить от иммунного ответа.

И какая ситуация с ковидом? Если возможны повторные заражения у переболевших — значит, и вакцины бесполезны?
Нет, не значит. С иммунитетом, скорее всего, все будет в порядке — по крайней мере в перспективе полугода — года. Что будет дальше, ученые прогнозировать не хотят, но из общих соображений мы знаем, что если проблемы и возникнут, то почти наверняка они будут связаны не с плохой иммунной памятью, а с изменением самого вируса.
Теперь подробнее. Уровень антител к SARS-CoV-2 действительно со временем постепенно уменьшается. Это показано уже в нескольких исследованиях (например, 1, 2, 3, 4, 5), где ученые наблюдали в течение нескольких месяцев за динамикой иммунного ответа у переболевших. По вакцинированным такого рода исследований нет, просто потому что после начала вакцинации прошло не так много времени. Однако в первом приближении можно считать, что у них иммунитет будет вести себя так же или даже более активно: во-первых, это справедливо для многих других инфекций, во-вторых, у 100% вакцинированных против SARS-CoV-2 вакцинами Pfizer/BioNTech, Moderna и «Спутник V» наблюдается выработка антител, причем часто в больших количествах, чем у переболевших.
Одно из самых подробных подобных исследований длительности иммунитета было недавно опубликовано группой Шайна Кроти из Калифорнийского университета в Science. В нем, в отличие от нескольких предыдущих, ученые проследили за эволюцией не только антител, но и четырех важнейших типов иммунитета в течение полугода и более (антитела в плазме, B-клетки памяти, киллерные Т-клетки, непосредственно уничтожающие зараженные вирусом клетки организма, хелперные Т-клетки, которые регулируют этот процесс, помогая Т-киллерам).
Из результатов этого исследования можно вынести два важнейших факта.
- Во-первых, ученые подтвердили и наглядно показали, что реакция на ковид у разных людей отличается гораздо больше, чем состояние иммунитета у одного и того же человека непосредственно после инфекции или много (до восьми) месяцев спустя. Это и качественные, и количественные отличия: у кого-то сильно активируются Т-киллеры, у кого-то вырабатывается больше антител, но в целом почти у всех реагируют все изученные ветви иммунной защиты и эта реакция не исчезает вдруг сама по себе через полгода — у 95% переболевших к концу исследования «работало» по крайней мере три линии защиты.
- Во-вторых, оказалось, что несмотря на небольшое, но заметное падение как по антителам, так и по T-клеткам не снижается уровень B-клеток — тех самых, которые способны реактивироваться при новом столкновении с инфекцией. В исследованном масштабе времени их становится только больше. Это означает, что никаких объективных оснований считать, что иммунитет к SARS-CoV-2 может вдруг сам по себе исчезнуть, просто нет. Тем более что ковид, как подчеркивают авторы, относится к довольно медленно протекающим инфекциям, а значит, при повторном заражении B-клетки будут иметь вполне достаточно времени для реактивации и производства большого количества антител. Если же взглянуть на совсем другую часть иммунитета — время полужизни Т-киллеров, — то и она не дает поводов для беспокойства: определенное время полужизни меньше, чем для оспы, но очень похоже на соответствующий параметр для желтой лихорадки (а вакцина против этого вируса дает пожизненный иммунитет).
В заключение авторы оговариваются, что поскольку те самые «корреляты защиты», о которых говорилось выше, для COVID-19 еще не установлены, то формально надежных выводов о будущем иммунитета для переболевших сделать нельзя. Однако ясно, что общая картина не сильно отличается от других вирусных инфекций, иммунитет к которым бывает пожизненным, так что «прочный иммунитет против вторичного заболевания COVID-19 возможен у большинства людей» — заключают исследователи.
А против новых вариантов SARS-CoV-2 вакцины подействуют?
К сожалению, не против всех одинаково эффективно. О новых вариантах коронавируса «Медуза» не так давно уже писала, и главное, что там сказано, по-прежнему остается актуальным: сейчас действительно уже есть несколько вариантов SARS-CoV-2, которые доказанно обладают особыми свойствами, в том числе большей заразностью, повышенной летальностью и способностью частично уходить от иммунитета. Основные и самые изученные — это британский (B.1.1.7), южноафриканский (B.1.351) и бразильский (P.1) варианты. Хотя сейчас постоянно регистрируются и другие, в чем-то схожие с этими тремя линии эволюции вируса (актуальную инфографику можно посмотреть здесь).
Есть несколько работ, в которых активность антител, вырабатываемых в ответ на существующие вакцины, проверяется в отношении новых вариантов вируса (1, 2, 3). Для британского варианта снижения способности «связывать» вирус ученые не наблюдают, однако в случае южноафриканского и бразильского такое снижение довольно значительно. Последние варианты схожи между собой наличием мутации E484K, которая, по-видимому, имеет ключевое значение для способности уходить от антител к классическому коронавирусу. Ее независимое возникновение было показано уже в нескольких линиях.
Так, в свежей работе оксфордских иммунологов, опубликованной в Cell, ученые впервые напрямую сравнили необходимые для нейтрализации вируса титры антител у привитых двумя вакцинами: Pfizer/BioNTech и AstraZeneca. Оказалось, что против южноафриканского нужно как минимум в 7,6 или даже 9 раз больше нейтрализующих антител (для вакцинированных Pfizer/BioNTech и AstraZeneca соответственно), чем против «обычного», уханьского варианта вируса. Перевести это снижение эффективности антител в снижение эффективности самих вакцин по какой-то формуле невозможно — как мы уже сказали, из-за пробелов в знаниях о коррелятах защиты для ковида. Однако разумно предположить, что именно этим объясняется низкая эффективность вакцины AstraZeneca, которую она показала в ЮАР.
Сейчас можно надеяться на то, что даже в случае инфекции новым штаммом старая вакцина будет защищать человека от тяжелого течения болезни. Однако надежных данных, говорящих об этом, пока нет. В любом случае производители вакцин уже сейчас готовятся к распространению новых мутаций и прорабатывают механизмы ускоренного обновления своих препаратов.
И что в итоге?
На сегодня мы знаем, что уровень антител к коронавирусной инфекции после заболевания со временем действительно падает (хотя и не очень быстро), однако клетки памяти, способные реагировать на повторное заражение, сохраняются. Повторные инфекции уже известны, но по-прежнему остаются очень редкими. При длительном и подробном изучении реакции иммунной системы ученые видят ответ, очень похожий на тот, что сопровождает реакцию на другие вирусы, иммунитет к которым бывает пожизненным. То есть потенциально вакцинный иммунитет может быть очень длительным — но зависеть он будет не от самих вакцин, а от того, как будет меняться вирус.
И действительно, уже сейчас есть несколько вариантов SARS-CoV-2, которые частично «уходят» от иммунитета — он в разы слабее, если сталкивается с этими новыми вариантами. Производители вакцин начинают учитывать это обстоятельство и готовят «апдейты» своих вакцин. Дальнейшее развитие пандемии будет зависеть от того, что будет происходить быстрее: всеобщая вакцинация или появление новых вариантов SARS-CoV-2, уходящих от уже существующих вакцин. В любом случае это дополнительный аргумент в пользу того, чтобы максимально наращивать скорость вакцинации, а людям соблюдать хотя бы часть из ограничений даже после прививки, которая может не сработать против новых вариантов.
Александр Ершов